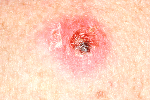
FDA одобрило препарат для лечения рака кожи
30 января 2012 г. Управление по контролю за пищевыми продуктами и лекарственными средствами США (Food and Drug Administration — FDA) одобрило препарат Erivedge (висмодегиб, «Roche») для лечения базально-клеточной карциномы — одного из наиболее распространенных злокачественных новообразований кожи. Это лекарственное средство предназначено для применения у взрослых, которым не показано оперативное вмешательство или лучевая терапия, а также для тех пациентов, у которых выявлены метастазы в других органах. В ходе многоцентрового клинического исследования при участии 96 пациентов с метастазирующей базально-клеточной карциномой были оценены эффективность и профиль безопасности Erivedge. Согласно результатам исследования, у 30% больных, применявших Erivedge, отмечалось сокращение объема, а у 43% — полное или частичное исчезновение злокачественных новообразований.
Умный массажер Xiaomi Mijia Smart Head Massage Comb оценили …
Компания Xiaomi выпустила на домашний китайский рынок умную массажную расчёску Mijia Smart Head Massage C…
Компания Xiaomi выпустила на домашний китайский рынок умную массажную расчёску Mijia Smart Head Massage C…
Пересадка волос без риска: почему анализы и врачи важнее цен…
Проблема выпадения волос знакома миллионам мужчин по всему миру. По статистике, пятеро мужчин из ста нужд…
Проблема выпадения волос знакома миллионам мужчин по всему миру. По статистике, пятеро мужчин из ста нужд…
Почему люди читают гороскопы и как астрология влияет на реше…
Миллионы людей ежедневно открывают гороскопы в газетах, приложениях и на сайтах. Кто-то относится к эт…
Миллионы людей ежедневно открывают гороскопы в газетах, приложениях и на сайтах. Кто-то относится к эт…
LED-маска Dreame Chrona Photon, триммер Dreame T3 и стайлер …
Dreame анонсировал в России три новых устройства для персонального ухода: интеллектуальный стайлер AirSty…
Dreame анонсировал в России три новых устройства для персонального ухода: интеллектуальный стайлер AirSty…